
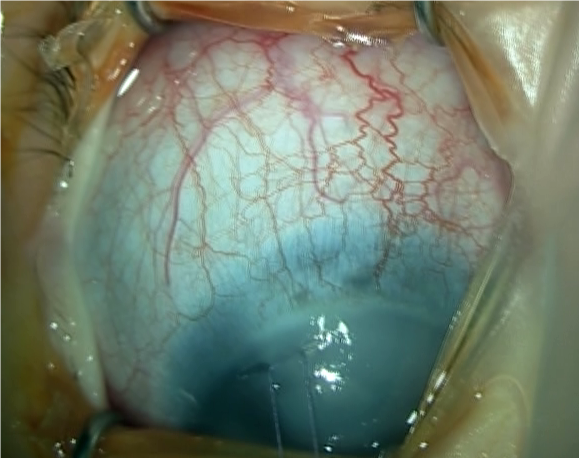

Yaş |
Minimum GİB (mmHg) | Maksimum GİB (mmHg) |
| 1 yaş altı | 8,4 | 9,4 |
| 1-2 yaş | 9,4 | 10,2 |
| 2-3 yaş | 10,4 | 11,1 |
| 3-4 yaş | 10,9 | 12,0 |
| 4-5 yaş | 11,6 | 13,1 |
| 5-6 yaş | 12,2 | 14,2 |

Yaş |
Normal | Şüpheli |
| Doğum –ilk 6 ay | 9,5-11,5 mm | >12 mm |
| 1-2 yıl | 10-12 mm | >12,5 mm |
| >2yıl | < 12 mm | >13 mm |
| Yaş | Normal | Şüpheli |
| Doğum –ilk 6 ay | 9,5-11,5 mm | >12 mm |
| 1-2 yıl | 10-12 mm | >12,5 mm |
| >2yıl | < 12 mm | >13 mm |

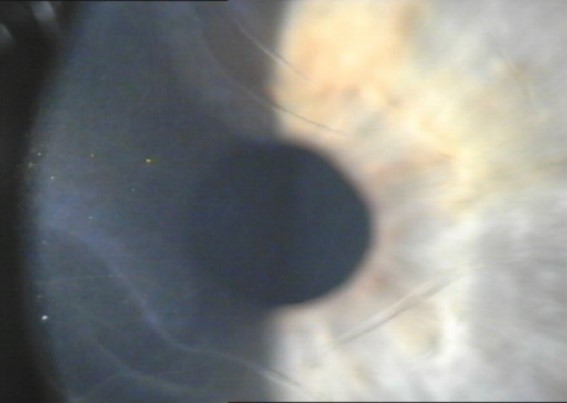

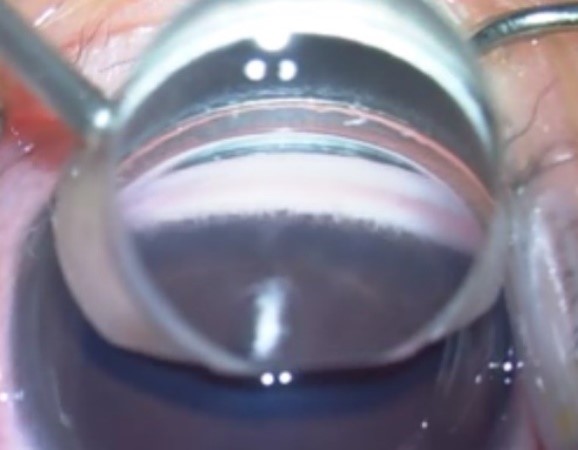
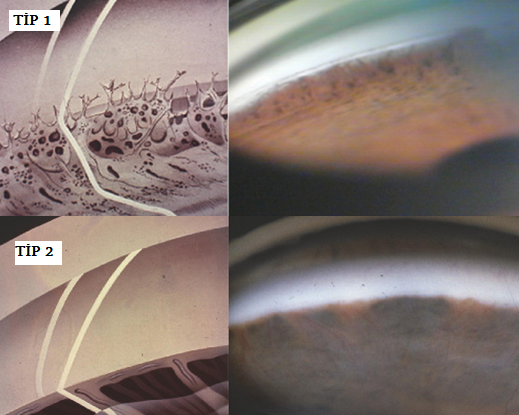
| Tip I ÖKA | Tip 2 ÖKA |
| Patolojik mezodermal kalıntı var | Bariz yüksek iris yapışıklığı var |
| AXL <23 mm | AXL >23 mm |
| Kornea çapı <13 mm | Kornea çapı >13 mm |
| Tercihan trabekülotomi ya da gonyotomi | Kombine cerrahi (Trabekülotomi+trabekülektomi) |