Endoftalmi
Prof. Dr. Selim Doğanay
Endoftalmi göz içi boşluğunun enflamatuar hastalığıdır. Genellikle enfeksiyöz nedenlerle oluşabilmesine karşın enfeksiyoz olmayan nedenlerden dolayı da oluşabilmektir. Panoftalmi terimi ise gözün tüm dokularının enflamatuar duruma eşlik etmesi olarak tarif edilir. Son yıllarda katarakt cerrahisi ve vitreoretinal cerrahide kesilerin küçülmesi, glokom cerrahilerinde mikroinvazif girişimler, kullanılan göz içi lenslerinin önceden yüklenmiş enjektör sistemlerinde kullanımı, cerrahi sterilizasyondaki teknolojik gelişimler, tek kullanımlık alet ve malzemelerin kullanım alanına girmesi, medikal ve ilaç sanayi alanlarındaki gelişmeler, endoftalmi oranlarında ciddi düşüşe neden olmuştur. Tüm bunlara rağmen endoftalmi, göz cerrahilerinde, hastanın ve göz cerrahının kaçınmak için gayret sarf ettiği korkutucu bir sorun olarak güncelliğini korumaktadır.
Enfeksiyöz endoftalmiler göz cerrahileri sonrası nadir görülmesine karşın gözde kalıcı görme hasarı ve gözün kaybına kadar giden durumlara yol açtığından, gerek göz doktorları gerekse hasta açısından can sıkıcı klinik bir durumdur. Ayrıca cerrah ve çalıştığı kurum açısından da ciddi medikolegal problemlere neden olabilmektedir.
Bu derlememizde aslında çok farklı klinik tablolarla karşımıza çıkabilen endoftalmi klinik durumunu, ameliyat sonrası gelişen enfeksiyöz endoftalmi açısından; profilaksi, klinik bulgular, risk faktörleri, tedavide medikal ve cerrahi yaklaşımlar ve kişisel deneyimler başlıkları sınırlı tutularak değerlendirilecektir.
Enfeksiyöz endoftalmi profilaksisi
Cerrahi endoftalmi profilaksisinde birçok yöntem tarif edilmektedir. Özellikle göz içi cerrahilerinde uygulanan endoftalmi profilaksi yöntemleri son yıllarda endoftalmi oluşumunu ciddi oranda azaltmıştır.
Kronolojik olarak baktığımızda, povidone-iodine kullanımı hala cerrahi profilakside önemini devam ettirmektedir. Povidine-iodine mükemmel bir anti septik olup, göz ameliyatları öncesi cerrahi alanın %10’ luk povidine-iodine solüsyonu ile temizlenmesi ve konjonktivaya %5 lik povidine-iodine uygulaması günümüzde yaygın olarak kullanılmaktadır. Yapılan bir araştırmada; ameliyat öncesi %5’ lik povidone-iodine uygulaması ile gümüş protein solüsyonunun (Argyrol) konjonktivaya uygulaması karşılaştırıldığında %5’ lik povidone-iodine lehine belirgin şekilde kültür pozitif endoftalmilerin azaltıldığı gösterilmiştir.1 Endoftalmilerin ana kaynağını oluşturan konjonktival flora elamanlarının azaltılmasını inceleyen bir çalışmada; ameliyattan 3 gün önce topikal neomisin sülfat ve cerrahi esnasında %5 povidine iodine kullanımının konjonktivada %83 oranında sterilizasyon sağladığı gösterilmiştir.1 Povidine-iodine sadece bakterilere karşı değil virüslere, mantarlara, protozoalara ve sporlara karşıdada etkili bir antiseptiktir.2 Göz alanının dreplemesini takiben konjonktival alana uygulanan %5 lik povidine-iodinin, bol göz içi kullanımına uygun sıvı ile oküler cerrahiye başlamadan önce alandan uzaklaştırılması önemlidir. Povidine- iodine endotele toksik etki göstermektedir.
Ciulla ve arkadaşları kanıta dayalı literatürlerin gözden geçirildiği derlemede endoftalmi profilaksisinde ameliyat öncesi povidine-iodine kullanımının tek en etkili yol olduğunu belirtmektedir.3 Nenwitch ve arkadaşlarının çalışmasında %1 betadinin ameliyattan 1 dakika önce konjonktivaya damlatılmasının endoftalmi oranını % 0.17’ den % 0.065 indirildiğini belirtmektedirler.4
Birçok göz hekimi herhangi bir risk faktörü olmamasına karşın elektif göz içi cerrahileri öncesi topikal antibiyotik kullanımını önermektedir. Topikal kullanılan bir antibiyotiğin enfeksiyonu önleyebilmesi için kullanımı sonrasında, minimal durdurucu konsantrasyonun üstüne çıkması gerekmektedir.5 Ancak ameliyat öncesi kullanılan topikal antibiyotiklerin kullanımı ile ilgili şu anda çok kesin bir cevap bulunmamaktadır. Amerikan katarakt cemiyetinin 2014 yılında yaptığı bir değerlendirmede toplam 7767 hekimin %85 i ameliyat öncesi topikal antibiyotik kullandığını ifade etmiştir. Bu hekimlerin %48’ i ameliyattan 3 gün önce, %32’si 1 gün önce, %20’ si ameliyat günü topikal antibiyotiğe başlamışlardır.6 Geriye dönük olarak yapılan bir çalışmada 42426 göz değerlendirilmiştir. Bu çalışmada; olgular ameliyattan bir gün önce ameliyat olacakları göze 6-8 defa/gün olacak şekilde topikal siprofloksasin damlatılmış ve olgulara sistemik antibiyotik, ameliyat sonunda intrakameral ve subkonjonktival antibiyotik kullanılmamış. Sonuçta bu olgularda endoftalmi oranı %0.09 olarak tespit edilmiştir.7 Bu oran ESCRS endoftalmi çalışmasındaki sub-grupta intrakameral antibiyotik alanlarda %0.075 olarak gerçekleşmiştir.7 Ta ve arkadaşlarının yaptığı bir çalışmada ameliyat öncesi 3 gün ofloksasin kullanımının ameliyattan 1 saat önce antibiyotik kullanımına oranla konjonktiva bakteriyal florasını ciddi oranda azalttığını göstermişlerdir.8
ESCRS endoftalmi çalışmasındaki veriler plasebo grubuna oranla labaratuar olarak doğrulanan endoftalmi olgularının, katarakt cerrahisinden 1 saat önce 2 damla levofloksasin kullanan gruba oranla plasebo grubunda endoftalmi riskinin arttığı bulunmuş ancak bu sonuçlar istatiksel olarak anlamlı bulunmamıştır.5,9 Özellikle 4. Kuşak kinolonların, levofloksasine oranla daha geniş spekturumlu etki, daha güçlü ve gram pozitif bakterilere daha etkili olması, göze penetrasyonunun daha iyi olması yanında resistan oluşumunun daha azalması gibi birçok avantajı bulunmaktadır. Kinolon grubundaki ilaçlara bakıldığında yapılan çalışmalarda moxifloksasinin; gatifloksasin, ciprofloksasin, ofloksasin ve levofloksasine oranla antibakteriyal etkinliğinin ve oküler konsantrasyonunun daha fazla olduğu ortaya konmuştur.10-12 2008 yılında Vasavada ve arkadaşları ameliyat öncesi iki ayrı yolla moxifloksasin kullanımını karşılaştırmışlardır. Bir grupta ameliyattan 1 gün önce günde 4 kez moxifloksasin ve ameliyattan 2 saat önce ek olarak 1 damla daha moxifloksasin kullanılmış, diğer gruba ise ameliyattan 2 saat önce 1 damla, bir saat önce ise 15 dakika aralıklarla moxifloksasin damlatılmıştır. Sonuçta ameliyattan 2 saat önce başlanan ve 1 saat önce 15 dakikada bir damlatılan grupta ilacın önkamera konsantrasyonunun S.epidermidis için gerekli bilinen minumun baskılayıcı konsantrasyonunun daha da üstüne çıktığı bulunmuştur.13 Bu şonuçlara rağmen Ciulla ve arkadaşlarının sistematik bir gözden geçirme yazısında ameliyat öncesi antibiyotik kullanımının bilimsel olarak profilakside doğrulanmadığı belirmektedirler.3 2007 ESCRS çalışmasında ameliyat öncesi antibiyotik kullanımı bir opsiyon olarak düşünülebileceği belirtirken Fransız ekolü endoftalmide topikal antibiyotik kullanımını önermemektedirler.14-15 Bununla beraber ameliyat öncesi rutin antibiyotik kullanımı ameliyat maliyetlerin artması, antibiyotik direnci ve kullanılan antibiyotiklere karşı alerjik reaksiyonların gelişimi gibi bazı problemleride beraberinde getirmektedir.
Geniş prospektif çalışmalarda ameliyat öncesi antibiyotik kullanımının endoftalmi riskini azalttığı doğrulanamamıştır. Ameliyat öncesi kullanılan antibiyotik göz florasını tamamen steril hale getiremediğine göre endoftalmi olgularınıda tamamen ortadan kaldırmak mümkün olmayacaktır. Bununla beraber gerek medikolegal açıdan gerekse riskli olgularda cerrah mediko-legal açıdan kendini koruması açısından ameliyat öncesi 2-3 gün geniş spekturumlu topikal antibiyotik kullanımını düşünebilir. Özellikle kullanılması planlandığında antibiyotik seçeneği bakterisidal etkiye sahip gram pozitif bakteri, gram negatif bakteri, stafilokolar ve psodomonaslara etki eden spekturuma sahip bir antibiyotik seçilmesinin yerinde olacağı düşünülmektedir.3 Bu amaçla günümüzde ameliyat öncesi kullanımına en uygun antibiyotik 4. Kuşak florokinolon grubundan moxifloksasindir.
Sistemik antibitotik kullanımı: Schmitz 300000 olguda katarakt cerrahisi öncesinde sistemik antibiyotik kullanımının ek bir fayda sağlamadığını belirtmiştir. Genel kanıda endoftalmi profilaksisinde sistemik antibiyotik kullanımı konusu tartışmalı olmakla beraber önerilmemektedir.16
İntrakameral antibiyotik kullanımı: ESCRS endoftalmi çalışma grubunun 16000 olgu üzerinde yaptığı çalışmada 4 alt grup oluşturulmuştur. Bu gruplar; ameliyat sırasında antibiyotik almayanlar, ameliyat sırasında topikal antibiyotik olarak levofloksasin kullanılanlar, ameliyatta sefuroksim intrakameral ve topikal levofloksasin kullanılanlar ve sadece sefuroksim intrakameral kullanılan olgulardan oluşmaktadır. Bu gruplarda endoftalmi oluşma oranlarına bakıldığında intrakameral sefuroksim kullanılmayan grupta endoftalmi 5 kat daha fazla ortaya çıkmıştır (%0.345-%0.062). Shorstein ve arkadaşları 16264 olguluk değerlendirmelerinde; %78 olgu intrakameral antibiyotik kullanılmış (%84 sefuroksim, %15 moxifloksasin) ve çalışma sonunda intrakameral antibiyotik verilen grupta verilmeyenlerden 13 kat daha az endoftalmi meydana gelmiştir.17-18 İspanyol ekolünün 10 yıllık prospektif çalışmasında, 13000 olguda intrakameral sefuroksim kullanılanlarda %0.043, kullanılmayanlarda endoftalmi oranı %0.59, Fransız ekolünün çalışmasında 5000 olguda sefuroksim intrakameral kullanılanlarda endoftalmi oranı %0.044 iken ilaç almayanlarda %1.23 olarak bulunmuştur.19-20 Tan ve arkadaşları 11 yıllık çalışmalarında 50000 olguda sefazolin intrakameral kullanımının (1mg-0,1ml) endoftalmi oranını %0.064’ den %0.01 e indirdiğini bildirmektedirler.21 Sefazolin sefuroksim ve seftazidimin intrakameral kullanımının merkezi retina kalınlığına ve endotel hücrelerine yan etki profili olmadığı gösterilmiştir.22 Bununla beraber moxifloksasin sefuroksime oranla daha geniş spekturumlu bir ilaç olması nedeni ile son zamanlarda kliniklerde sefuroksime alternatif olarak kullanılmaktadır. Birçok çalışmada moxifloksasinin güvenli olan dozu araştırılmıştır (0,1mg/0,1ml, 0,5mg/0,1ml, 250 mikrog/0,05 ml). Moxifloksasin intrakameral kullanımının retinada veya kornea entotelinde bir hasar meydana getirmediği birçok çalışmada gösterilmiştir.23-25 Vancomisin 1mg/0,1 ml dozunda intrakameral kullanımı mevcuttur. 16000 olguluk bir çalışmada endoftalmi riskinin 1mg/0,1ml vakomisinin intrakameral kullanımı ile %0,3 den %0,008’ e indiği belirtilmektedir. Vancomisin gram pozitif bakterilere oldukça ekili olup aynı zamanda metisiline dirençli stafilokoklarada etkili bir ilaçdır. Ancak gram negatif bakterilere etkisi mevcut değildir. İntrakameral kullanımına bağlı makuler ödem oluşturması ve spekturumun sınırlı olması kullanımının yaygınlaşmasına engel olmuştur.24 Bir başka çalışmada intrakameral vancomisinle moxifloksasinin endoftalmi önlenmesinde birbirine bir üstünlük oluşturmadığı belirtilmektedir.26
Endoftalminin klinik bulguları
Enfeksiyöz endoftalmi göz içi herhangi bir ameliyat sonrası meydana gelebilir. Katarakt cerrahisi sonrası enfeksiyöz endoftalmi oluşma riski değişik yayınlarda %0,07 ile %0,13 oranları arasında bildirilmektedir.27-29 Pars plana vitrektomi sonrasında endoftalmi oranları %0,04 ile %0,07 oranlarında bildirilmektedir.27,30
Özellikle katarakt cerrahisinde fakoemülsifikasyonun kullanıma girmesi ile endoftalmi oranlarında belirgin bir azalma olmuştur. Bu azalmanın göz florasından veya dışarıdan ekstrakapsüler katarakt cerrahisinde, ameliyat yönteminin özelliği nedeni ile daha fazla mikrobiyal etkenin göz içine girişi ile açıklanmaktadır. Fakoemülsifikasyon cerrahisinde endoftalminin daha az görülmesinin nedenleri; fakoemülsifikasyon cerrahisinin eksrakapsüler katarakt cerrahisine oranla daha kapalı bir sistem olması, sıvı akışı nedeni ile dışarıdan bulaşın minimal olması ile açıklanabilir. Yapılan bir çalışmada ekstrakapsüler katarakt cerrahisinde %28.2 oranında göz içinin kontamine olduğu belirtilirken fakoemülsifikasyonda bu oran %7.6 olarak verilmektedir.31
Her ne kadar radial keratotomi veya şaşılık operasyonları göz dışı cerrahileri olarak kabul edilse bile bu olgularda da endoftalmi riski mevcuttur. Bu risk şaşılık opererasyonlarında skleral perforasyon, radial keratotomide ise korneal kesiye bağlı oluşabilecek perforasyon veya keratite sekonder gelişebilir.32-33
Penetran keratoplasti sonrasında enfeksiyöz endoftalmi oranları %0,11 ile %0,18 arasında verilmektedir. Bu oranlar kombine katarakt ve penetran keratoplastide %0,19, filtran glokom cerrahisinde %0,06-%1.8 arasında bildirilmektedir.27,34-35 İntravitreal enjeksiyonlar sonrasıda 0.019-%0.07 oranlarında ciddi endoftalmi olguları gelişebilmektedir.36 (fotoğraf 1)
Enfeksiyöz endoftalmilerde mikroorganizmaların kaynağı genellikle göz kapağı, lakrimal kese, konjontivada kolonize olan mikroorganizmalardır. Endoftalmiye neden olan mikroorganizmaların %90’nı gram pozitif aerobik bakteriler, %7 sini, gram negatif bakteriler ve %3’nü mantarlar oluşturur.37 Bununla beraber anerobik bakteriler de enfeksiyöz endoftalmilere neden olabilirler. Mantarlar nadir olsada enfeksiyöz endoftalmilerin nedeni olabilmektedir. Katarakt cerrahisi sonrası epidemik mantar enfeksiyonlarına bağlı endoftalmi serileri literatürde bildirilmiştir.38-40
Enfeksiyöz endoftalmilerin hasta kaynaklı nedenlerin yanısıra ameliyatta kullanılan sıvılar, viskoelastikler, sterilizasyonu problemli aletler, donor kornea, havadan bulaşlar kaynak oluşturabilmektedir. Bu etkenler endoftalmi patlamalarına neden olabilmesi açısından çok iyi değerlendirilmeli ve dikkate alınmalıdır.
Akut endoftalmiler ameliyat sonrası 6. haftaya kadar oluşabilmektedir. Başlangıç bulguları; görme keskinliğinde akut başlayan azalma, afferent pupiller defekt, ağrı, hipopiyon, korneal ödem, korneal infitrat, önkamerada fibrin reaksiyonu, vitreusta inflamasyon, retinit ve/veya retinal periflebit olarak sayılabilir. Göz eksternal olarak değerlendirildiğinde siliyer enjeksiyonla beraber kırmızı göz, kemozis, kapaklarda ödem oluşması görülebilir. Eğer tablo eksternal göz dokularınada yayılmışsa göz hareketlerinde belirgin kısıtlanma, propitozis tabloları endoftalmiye eşlik edebilmektedir. Enfeksiyoz endoftalmilerde en sık izole edilen bakteri s.epidermidis olarak gösterilmektedir. S.epidermidis enfeksiyonlarına bağlı oluşan endoftalmiler, s.aerosus, stereptokok ve gram–rod enfeksiyöz etkenlerine göre daha az virulandır. P. acnes ve mantarlar gecikmiş endoftalmi etkeni olup akut başlangıçlı endoftalmi etkenleride olabilmektedir.41-42
Basilyus türleri nadiren ameliyat sonrası endoftalmi etkeni olup genellikle travmatik göz yaralanmaları sonrası oluşan endoftalmi etkenleri arasında gösterilmektedir. Özellikle Bascilluus cereus endoftalmileri tedaviye yanıt ve görsel sonuçlar açısından en kötü sonuçların alındığı enfeksiyöz endoftalmi nedenlerindendir.
Endoftalmi vitrektomi çalışması (EVS), endoftalmi olgularının %69’ unda mikrobiyolojik olarak etkenin saptandığını ortaya koymuştur. Bu etkenlerin %70’ i koagülaz negatif mirokoklar (genellikle s.epidermidis), %10 s.aerosus, %9 stereptokoklar, %2 enterokoklar, %3 diğer gram + türler, %6 diğer gram – türler olarak vermektedir.43-45
EVS çalışmasında; klinik bazı bulgulara bakılarak kültür sonuçlarının öngörülebileceği belirtilmektedir. Örneğin; indirekt oftalmoskopik muayenede eğer retina damarları görülüyorsa bu olgularda gram – bakteri üremesi gerçekleşmemiştir. Özellikle diyabetik olgularda %58.6 gram +, koagülaz – mikrokoklar bakteriler, diyabetik olmayanlara oranla daha fazla tespit edilmiştir (diyabetik olmayanlarda %45). Korneal infiltrat varlığı, katarakt kesi yeri anormalliği (iris ve ve vitreusun korneal girişten inkarsere olması), afferent pupiller defekt, retina kırmızı reflesinin alınamaması, kişinin sadece ışığı fark etmesi, cerahi müdahaleden sonraki 2 gün içinde enfeksiyonun gelişmiş olması, gram + ve koagülaz – mikrokoklara oranla özellikle gram - organizmaları düşündürmelidir. Bu çalışmada hipopiyon seviyeleri; gram - 1.7 mm, gram + koagülaz – etkenlerde 1.2 mm, olarak bulunmuştur. Kapaklarda ödem varlığı daha çok diğer gram+ organizmaların etken olduğu görülmüştür. Lokosit sayımının 10000 üzerinde olması diğer gram+ bakterilerin etken olduğu endoftalmilerde 3 kez daha fazla olguda görülmüştür. Ağrının varlığı kültür sonucu için prediktif bir faktör olmadığı bulunmuştur. Korneal inftratın varlığı yara yeri anormalitesi kırmızı reflenin olmaması, aferent pupiller defektin varlığı enfeksiyonun cerrahi sonrası ilk 2 günde oluşması, %50 ve daha yüksek olasılıkla gram – veya diğer gram + organizma etkeni olduğunun göstergesi olarak bulunmuştur. Sonuç görme keskinliğinin 20/100 ve üzerinde olduğu olgularda izole edilen organizmalar gram + koagülaz negatif mikrokoklar %84, s.aerosus %50, stereptokoklar %30, enterokoklar %14, gram – mikro organizmalar %56, olarak bulunmuştur. EVS sonuçlarına göre gram boyanmadan ziyade koagülaz – mikrokokların sonuç görme keskinlikleri daha kötü bulunmuştur. Bununla beraber endoftalmi tespit edildiğinde alınan görme keskinliği ölçümünün iyi olması, mikrobiyolojik etkenlerden daha önemlidir. Bir başka deyişle organizma ne olursa olsun, görme keskinliği başlangıçta ne kadar iyi ise vitrektomi sonrasında elde edilen sonuç görme o kadar iyi olarak bulunmuştur.46

Fotoğraf 1: İntravitreal ranizumab enjeksiyonu sonrası gelişen acinetobacter baumannii neden olduğu fulminan endoftalmi olgusu; rutin endoftalmi yaklaşımı tedavisine rağmen tedavide başarı sağlanamadı. Sonuçta; eviserasyon ameliyatı yapılmak zorunda kalındı.
Ameliyat sonrası endoftalmi sınıflaması
Tip |
Ortaya çıkış zamanı |
Muhtemel etken |
Sıklıkla beraber olduğu cerrahi |
Hirpopiyon ve ağrı |
Fulminan |
<4 gün |
Gram-bakteri P.aeruginosa
S.pneomonia
S.aureus
|
katarakt cerrahisi |
Çok sık |
Akut |
2-11 gün
(ortama 5-7 gün) |
Koagülaz – Stafilokok
S.aeurosus, stereptokok
Türleri, Gram - bakteri
|
katarakt cerrahisi sonrası arka kapsülde peynirimsi beyaz kalınlaşma, |
Çok sık |
Subakut/geçikmiş başlangıç |
2 hafta-aylar
(ortama 5-7 hafta) |
P.acnes, s.epidermidis, mantar(candida parapsilosis) Corynebacterium sp. |
katarakt cerrahisi arka kapsül rüptürü, vitreus kaybı, sekonder G.İ.L yerleştirilmesi |
Nadiren |
Kronik/geç başlangıç |
aylar-yıllar
(ortama >6 hafta) |
Stereptokok sp. Enterekok, H.influenza, stafilokok türleri
Mantar |
Filtre eden antifibrotik kullanılan blep, ince blep duvarı, kaçak olan kistik blep, katarakt cerrahisi |
Çok sık
Nadiren |
G.İ.L: göz içi lensi
Enfeksiyöz endoftalmi oluşumunda için risk faktörleri
Kültür pozitif enfeksiyöz endoftalmilerde primer kaynak genellikle göz yüzeyi ve göz adneks yapılarıdır. Yapılan bir çalışmada vitrektomi örneklerinden alınan sonuçlarla oküler flora arasında %82 uyum bulunmuştur.47 Endoftalmi için ameliyat öncesi risk faktörleri olarak; blefarit, konjonktivit, kanalikülit, dakriyosistit, lakrimal kanal tıkanıklıkları, kontakt lens kullanımı, diğer gözde oküler protez kullanımı48 kişinin immunsupresyonda olması ve diabetinin bulunması46,49 özellikle çocuklarda üst solunum yolu enfeksiyonları sayılabilir.50-51
Özellikle atopik dermatitli kişilerde ve keratokonjonktivit sikkalı olgularda yüksek oranda stafilokok kolonizasyonu oluşabilmektedir.52 Yapılan bir çalışmada sekonder göz içi yerleştirilmelerinde diğer göz içi cerrahilerine oranla daha yüksek oranda endoftalmi oluşumu bildirilmiştir.53 Sekonder göz içi lens yerleştirilmelerinde endoftalmi etkeni genellikle s. epidermidisdir. Transskleral sütürlü göz içi lensleri, polipropilen haptikli göz içi lensleri, göz içi ameliyatları öncesi kapak kenarı anormalliği olanlar, daha önceki giriş yerlerinden tekrar göz içine girilmesi, ameliyat sonrasında giriş yerlerindeki anormallikler ve defektler endoftalmi oluşumu için diğer risk faktörlerini oluşturur. Ameliyat sırasındaki risk faktörleri arasında; yetersiz kapak kenarı ve oküler yüzey desenfeksiyonu, ameliyatın uzaması, vitreus kayıpları, prolen haptikli göz içi lensleri, yetersiz ve uygun olmayan göz dreplemesi ve kirpiklerin ameliyat sahasında olması gibi etkenler gösterilebilir.54-57
Özellikle kullanılan yapışkanlı dreplerin kapak kenarlarını ve kirpikleri örtecek şeklilde iyi yapışması ve ameliyat sırasında bu yapışıklığın açılmayacak ölçüde sağlamlığı cerrahi alanın etkilenmemesi ve korunması açısından önemlidir. Polimer yüzeyler bakterilerin tutunmasında kolaylaştırıcı olduğu ve endoftalmide bir risk teşkil ettiği diğer taraftan heparin yüzeylerin bunun tam tersine yapışmayı engelliyerek bu riski azalttığı belirtilmektedir. Diğer taraftan önce yüklenmiş lenslerin kullanıma girmesi; özellikle katarakt cerrahilerinde lensin kartuşla yüklenmesi sırasındaki manipulasyonları en aza indirmiş olması, manuel katlama sırasında oküler yüzeyle lensin ilişki kurması gibi risk oluşturabilecek durumların meydana gelmesini sınırlamıştır.58-59
Penetran keratoplastilerde donor butonları endoftalmi kaynağı olabilmektedir. Bu nedenle kişisel uygulama olarak bu olgularda verici korneayı kullanmadan önce vancomisin 1mg/ml olacak şekilde ayarlanmış sıvılarda 10 dakika bekleterek kullanmakyayız. Bunun yanı sıra donor korneanın korunduğu sıvıları ve kullanılan kornea butonunu mutlaka kültüre yollamaktayız. Bu bize hem ameliyat sonrası oluşabilecek bir enfeksiyonun kaynağı hakkında ön bilgi sağlamakta hemde mediko legal açıdan önem arz etmektedir.
Ameliyat sonrasında en önemli risk faktörleri; yara yerinden kaçak olması, gömülmemiş dışarıdaki sütürler, sütür alımı, vitreusun yara yerine inkarsere olması, filtre eden bir blebin bulunması, özellikle bu blebin ince duvarlı kistik olması ve skleral tünel insizyonlar endoftalmi oluşumu için risk oluşturabilmektedir.60-66
Kronik enfeksiyöz endoftalmi
Kronik enfeksiyöz endoftalmi tanısı için, endoftalmi tablosunun ameliyat sonrası 6. haftadan sonra oluşması gerekmektedir. Kronik endoftalmide ensık izole edilen mikroorganizma s.epidermidis, p.acnes, mantarlar (özellikle candida türleri) anerobik streptokok türleri, aktinomiceş türleri ve nokardia asteroides’ dir. Özellikle p. acnes endoftalmileri tekrarlayıcı ameliyat sonrası inflamasyonlara neden olduklarından bazen enflamatuar reaksiyonlarla karışabilmektedir. Bu bakteriler özellikle kapsüler kese içerisinde kolonize olurlar ve beyaz kapsüler opasiteler meydana getirebilirler. Kültürlerde tespit edilmeleri uzun zaman alabilir. Özellikle bu sonuç için 2 hafta veya daha fazla bir zaman beklenebilir. Bu olgularda tedavide kapsülle beraber lensin alınması önerilmekle beraber bu işlem sonrasında bile tekrarlayıcı özelliğe sahip olabileceği bilinmelidir. Özellikle düşük dereceli üveit oluşturması ve topikal kortikosteroid kullanımına cevap alınması tipik özelliğini oluşturmaktadır. Bu olgularda; endoftalmide sık görülen ağrının nadir olması, katarakt cerrahisinde tam olarak alınamamış lens partiküllerine bağlı veya arka kapsül opasitesi için Nd-yag lazer sonrası görülen düşük dereceli üveit tablosunu düşündürmesi, teşhisin uzamasında etkili olabilir. Bu olgularda görülen enflamasyonun özelliği granulomatöz bir üveit tablosunu taklit etmesidir ve genellikle vitritis buna eşlik eder. Ancak bu olgularda arka kapsülde ve göz içi lensi üzerinde beyaz bir plağın görülmesi teşhis açısından düşündürücü olmalıdır. Bu beyaz plaklar özellikle periferde görülebileceğinden, şüphe duyulduğunda mutlaka pupilla tam dilate edildikten sonra dikkatli olarak muayene edilmelidir. Ancak beyaz kapsül plaklarının bakteriyel olduğu kadar, mantar enfeksiyonlarında da görülebileceği unutulmamalıdır.42,54,66-70 Mantar endoftalmilerinde beyaz inci tanesi şeklinde infiltratlar önkamerada ve vitreusta görülebilir. Hipopiyon sık olmasına rağmen granulomatöz bir inflamasyon genellikle görülmez.71-73
Trabekülektomi sonrası endoftalmi
Özellikle filtran cerrahilerden sonra haftalar hatta yıllar sonra fitran bleblere bağlı olarak endoftalmi tablosu oluşabilmektedir. Endoftalmi oranları %0.061-%1.8 oranları arasındadır. Filtran cerrahilerden sonra iki klinik tabloda enfeksiyon oluşur. Konjontivada oluşturulan blebin lokalize enfeksiyonu şeklinde olabilir. Bu tabloda enfeksiyon sadece bleb ve etrafı ile sınırlı olup vitreus boşluğu etkilenmemiştir. Diğer tabloda ise aylar veya yıllar sonrası oluşabilen bleble ilgili aynı zamanda vitreusunda tabloya eşlik ettiği endoftalmi tablosudur.74-76 Özellikle mitomisin c, 5-flurourasil gibi antiproliferatif ilaçların trabekülektomi başarısını artırmak amacı ile kullanıma girmesinden sonra, ince kistik bleplerin olduğu aynı zamanda seidel + olan olgularda bu risk artmaktadır. Yapılan bir çalışmada en sık rastlanan stereptokoklar %57, H-influenza %23 bulunmuştur. Diğer taraftan s.aerosus, psodomanas ve mantarlar ve diğer bakterilerde bleple ilgili endoftalmi oluşumuna neden olabilmektedir.74,76-79
Trabekülektomi sonrası endoftalmi için risk faktörleri arasında; inferior trabekülektomi, özellikle risk açısından önemlidir. Bunun nedeni olarak, mitomisin c kullanılan olgularda ince duvarlı ve avasküler bleplerin göz kırpılmasının kronik etkisiyle hasarlandığı ve bu bleplerden kaçak oluşma olasılığının artmasına ve sonuçta daha yüksek oranda endoftalmi oluşumuna neden olduğu bildirilmektedir.80 Diğer taraftan seton uygulamaları sonrasında da akut veya kronik endoftalmi oluşabilmektedir. İmplantın gerek konjonktivada gerekse sklerada meydana getirebileceği erezyonlar enfeksiyon açısından risk teşkil etmektedir.81-82 Filtran cerahi geçirmiş olgularda; kontakt lens kullanımı, dakriyosistit, konjonktivit, kontamine göz damlaları, üst solunum yolu enfeksiyonları endoftami gelişimi için risk faktörleri olarak gösterilmektedir.
Ameliyat sonrası oluşan endoftalmi etkeninin teşhisi
Ameliyat sonrası oluşan endoftalmi etkeninin hızlı ve doğru olarak tespit edilmesi tedavinin etkili ve doğru şekilde yapılmasını sağlamakta, sonuçta anatomik ve fonksiyonel başarı oranlarını yükseltmektedir. Özellikle moleküler biyolojik teknikler günümüzde etkenin doğru ve yüksek oranlarda tespitini mümkün kılmaktadır.
Endoftalmi örneklerinin toplanması teknikleri
Endoftalmi olgularında etkenin tespiti için önkamara sıvısı ve/veya vitreus örnekleri kullanılır. Bu örneklemeler gerek topikal gerekse sistemik veya intravitreal tedavi uygulamalarından önce alınmalıdır. Bu örneklemeler normal göz içi cerrahisi esaslarında olduğu gibi lokal alan antisepsisi ve dreplemeden sonra alınmalıdır. Bu amaçla korneal parasentezden önkamera sıvısı ve/veya vitreus boşluğundan vitreus sıvısı alınarak yapılır. Vitreus sıvısından alınan örneklerde etkenin ortaya çıkarılmasında, önkamera sıvısı örneklerine oranla daha yüksek oranda sonuç almak mümkündür. Vitreus örneklemesinde pars planadan yapılacak bir girişle alınan sıvı miktarı en az 200-300 mikro litre olmalıdır. Yöntem olarak 25 veya 27 g bir iğnenin pars planadan vitreus boşluğuna yönlendirilmesi ile ve iğnenin 2-3 cc lik enjektöre bağlanması ile basit bir girişimle gerçekleştirilebilir. Aynı girişten örnek alındıktan sonra planlanan antibiyotiklerin uygun dozda, vitreus boşluğuna verilmesi mümkündür. Bunun yanı sıra vitrektomi işlemi sırasında kasetten alınacak örneklerin değerlendirilmesi mümkündür. Ancak pür alınan örnek ve vitrektomi kasetlerinden alınan örneklerin beraber değerlendirilmesinde %57 oranında etken bulanabilirken bunların tek başına alınması durumunda: pür vitreus örneklemesinde %44, vitrektomi kasetlerinin tek başına değerlendirmesinde %49, oranında etken ortaya konabilmektedir.83-84
Konjontiva örneklemesi, etkenin tespiti açısından normal floranın tespiti nedeni ile klinik önemi bulunmamıştır. Alınan örnekler likid kültür ortamlarına (kan kültürü şişeleri, beyin kalp infüzyon besi alanı) steril şekilde alınmalıdır. PCR analizlerinde örnekler steril şekilde alınarak steril DNA tüplerine konulmalıdır. Moleküler analiz için minumum 50 mikrolitre örnek alınması önerilmektedir. DNA analizi için alınan örnekler steril ikincil taşıyıcılara konulur. Alınan örneklerin mikrobiyoloji labaratuvarına ulaştırılmasında 2 saat aşılmamalıdır. İnoküle edilen kültür ortamları 37 derecede saklanırken, PCR tüpleri 4 derecede 48 saat veya -20 derecede daha uzun süre bekletilebilir.
Kültür metodları
Alınan örneklerden 20 miro litrelik kısım 2 ayrı slayt kullanılarak 1 slatyta May-Grünwald Giemsa ile boyanır bu slaytta lokositler ve mantarlar değerlendirilir. 2. slayt da ise gram boyama yapılarak bakteri ve mantarlar direkt bakı ile mikroskop altında değerlendirilir. Bu yöntemlerle %19 oranında etken ortaya konabilir.85
Kullanılan diğer değerlendirme yöntemi beyin kalp infüzyon besi yeri, thioglycollate besiyeri, kanlı agar besi yeri, çikolatalı agar, MacConkey agar ve Sabouraud agar besi yerleridir. Örnekler bunların dışında kan kültürü şişelerinde değerlendirilir. Kan kültürleri klasik besi yerlerin göre daha yüksek duyarlılığa ve daha düşük kontaminasyona olanak sağlar. Kan kültür ortamları aerobic bakteri (staphylococci, streptococci, enterobacteria, vb.), özellikle anaerobic bakteri (Propionibacterium acnes) ve mantar (Candida spp.) tespitinde değerlidir. Özellikle mantar üremeleri için 2 haftalık bir süreç beklenmelidir. Bunun yanı sıra üreme durumunda antibiyogramların yapılarak etkili tedavinin yönlendirilmesi sağlanır
Moleküler biyolojik teknikler
Panbakteriyal PCR incelemeleri özellikle son yıllarda modern kliniklerde endoftalmi etkenlerinin tespitinde sık başvurulan yöntemlerden biridir. Bununla beraber spesifik PCR teknikleri panbakteriyal PCR tekniğine oranla daha hızlı ve daha duyarlı olarak etkeni ortaya koyabilmektedir. Bir diğer moleküler biyoloji metodu DNA microarray analiz metodudur.86
PCR metodlarında’da etkenin %100 tespit edilmesi mümkün olmamakla beraber diğer metodlara oranla daha duyarlı hızlı bir yöntem olduğu ortadadır. Bununla beraber kültür metodlarının ve antibiyogramın tam olarak yerini alamaz. Panbakterial PCR yöntemi ile intravitreal antibiyotik uygulamalarından sonra bile pür ve dilüe vitreus örneklerinden olguların %72’sinde bakteriyel etken tespit etmek mümkün olmaktadır. Bu nedenle altın standart olarak bu yöntemin uygulaması tüm endoftalmi olgularında tavsiye edilmektedir.87
Tedavi
Medikal tedavi
Medikal tedavide ameliyat sonrası endoftalmi şuçlarında en sık elde edilen etkenlerin gram + ve gram – mikroorganizmalar olması nedeni başlangıç antibiyotik tedavisi;
- Akut başlangıçlı ameliyat sonrası bakteriyal endoftalmide
- İntravitreal
Vancomisin 1 mg/0.1 ml
Ceftazidime 2.25 mg/0.1 ml veya amikasin 0.4mg/0.1 ml
Dexamethasone 0.4 mg/0.1ml (opsiyonal)
- Perioküler (subkonjonktival): opsiyonal
Vancomycin 25 mg
Ceftazidime 100 mg
Dexamethasone 12 mg ile 24 mg arası bir doz verilebilir
- Topikal: opsiyonal
Vancomycin 25 mg/ml saat başı gün boyunca
Ceftazidime 50 mg/ml saat başı gün boyunca
Topikal steroid ve sikloplejik damla 4x1
- Sistemik antibiyotik (genellikle kullanılmaz)
Ciddi enflamasyon ışık hissi düzeyinde görme keskinliği, hızlı başlangıçlı endoftalmile, glokom drenaj ameliyatı olanlar ve panoftalmi olgularında mutlaka başlanmalıdır.
Vancomycin 1gr /12 saat arayla intra venöz veya oral fluorokinlon (levofloksasin 500-750 mg günde 1 kez), son yıllarda özellikle göz içi geçişi iyi olan moxifloksasin tabletler (avelox 400 mg 1x1) kullanılmaktadır.
- Sistemik steroid kullanımı (opsiyonal)
prednisolone 1-2 mg/kg/gün-oral, Betamethasone 0.5-5 mg/kg/gün-oral, dexamethasone 0.5-5 /mg/kg/gün-oral
- Kronik ameliyat sonrası endoftalmi olgularında
- İntravitreal (bakteriyal etyoloji)
Vancomisin 1 mg/0.1 ml
Ceftazidime 2.25 mg/0.1 ml veya amikasin 0.4mg/0.1 ml
Dexamethasone 0.4 mg/0.1ml (opsiyonal), organizma tespit edilene kadar başlangıçta tedaviye eklenmemelidir.
- İntravitreal (fungal)
Voriconazole 0.1 mg/0.2 ml veya
Amphotericin 0.005 mg/0.1 ml
- Perioküler (subkonjonktival): opsiyonal.
Vancomycin 25 mg
Ceftazidime 100 mg
Dexamethasone 12 mg ile 24 mg arası bir doz verilebilir
- Topikal; rutin olarak kullanılmaz ancak özellikle kornea absesi, sütür absesi ve blebite bağlı endoftalmi olgularında kullanılmalıdır.
Vancomycin 25 mg/ml saat başı gün boyunca
Ceftazidime 50 mg/ml saat başı gün boyunca
Topikal steroid ve sikloplejik 4x1
- Sistemik (genellikle kullanılmaz)
Ciddi olgularda bakteriyal ve fungal endoftalmilerde başlanmalıdır
Konjonktival filtre eden bleblerde-Glokom drenaj implantarda meydana gelen endoftalmilerde
- İntravitreal
Vancomisin 1 mg/0.1 ml
Ceftazidime 2.25 mg/0.1 ml veya amikasin 0.4mg/0.1 ml
Dexamethasone 0.4 mg/0.1ml (opsiyonal)
- Perioküler (subkonjonktival): opsiyonal.
Vancomycin 25 mg
Ceftazidime 100 mg
Dexamethasone 12 mg ile 24 mg arası bir doz verilebilir
- Topikal
Vancomycin 25 mg/ml saat başı gün boyunca
Ceftazidime 50 mg/ml saat başı gün boyunca
Topikal steroid ve sikloplejik 4x1
- Sistemik
Ciddi enflamasyon ışık hissi düzeyinde görme keskinliği, hızlı başlangıçlı endoftalmilerde
İntravitreal antibiyotik ve antifungal ilaçların hazırlanması
Vancomycin (1mg/0.1 ml)
- 500 mg vancomycin flokonuna 10 ml injeksiyonluk %0.9 sodium chloride prezervan içermeyen sıvı veya BSS eklenerek toz halindeki ilacın çözünmesi sağlanır.
- Bu karışımdan 2 ml alınarak 8 ml BSS veya %0.9 sodium chloride prezervan içermeyen sıvı eklenir sonuçta 1 mg/0.1ml oran elde edilmiş olunur.
Ceftazidime (2.25 mg/0.1 ml)
- 500 mg ceftazidime ilaç alınır 10 ml injeksiyonluk %0.9 sodium chloride prezervan içermeyen sıvı veya BSS eklenerek toz halindeki ilacın çözünmesi sağlanır.
- Bu karışımdan 1 ml alınıp 1.2 ml BSS veya %0.9 sodium chloride prezervan içermeyen sıvı eklenir sonuçta 2.25 mg/0.1 ml oran elde edilmiş oluruz.
Amikacin 0.4 mg/0.1 ml
- 500 mg/2ml lik amikacin alınır. Buradan 0.16 ml çekilir (40 mg)
- Bu alınan 0.16 ml lik amikacin içine 9.84 ml enjeksiyonluk %0.9 sodium chloride prezervan içermeyen sıvı veya BSS eklenerek 0.4 mg/0.1 ml elde edilir.
Amphotericin B (Fungizone) 0.005 mg/0.1 ml
- 50 mg Amphoreticin ve ilaç alınır 10 ml enjeksiyonluk steril su (prezervan içermeyen)
- Bu karışımdan 0.1 ml alınarak 9.9 ml enjeksiyonluk steril su (prezervan içermeyen) eklenerek 0.005 mg/0.1 ml elde edilir.
Voriconazole 0.05 mg/0.1 ml
- 200 mg toz variconazole ilaç içerisine 19 ml enjeksiyonluk steril su (prezervan içermeyen) ile çözülür
- Bu çözeltiden 1 ml alınır ve 20 ml. enjeksiyonluk steril su eklenir (prezervan içermeyen) 0.05 mg/0.1 ml ilaç elde edilir.
Dexamethasone 400 mikrolitre/0.1 ml
- Bu ilaç 2 ml/8 mg hazır ampulleri vardır. Bu ampulden insülin iğnesine 0.1 ml çekildiğinde bu doz elde edilir.
Subkonjonktival antibiyotiklerin hazırlanması
| Antibiyotik |
Flakon |
Eklenecek volüm |
Enjeksiyon volümü |
Dozu |
Amikacin |
100mg/2ml |
0 |
0.5 ml |
25 mg |
Ampicillin |
1gr |
5 ml |
0.5 ml |
100 mg |
Clindamycin |
600mg/4ml |
0 |
0.33 ml |
50 mg |
Cephalothin |
1gr |
5 ml |
0.5 ml |
100 mg |
Ceftazidime |
500 mg |
2.5 ml |
0.5 ml |
100 mg |
Chloramphenicol |
1gr |
5 ml |
0.5 ml |
100 mg |
Gentamicin |
80 mg/2ml |
0 ml |
0.5 |
20 mg |
Methicillin |
1gr |
5 ml |
0.5 ml |
100 mg |
Vancomycin |
500 mg |
5 |
0.25 ml |
25 mg |
Tobramycin |
80 mg/2ml |
0 ml |
0.5 |
20 mg |
Cefazolin |
500 mg |
2.5 ml |
0.5 ml |
100 mg |
Eklenecek volüm: Nonbakteriyostatik steril su, mg: miligram, ml: mili litre
Fortifiye topikal antibiyotik hazırlanması
- Vancomycin 25 mg/ml
- 500 mg vancomycin flakonunun içerisine 20 ml. enjeksiyonluk %0.9 sodium chloride prezervan içermeyen sıvı veya Tears naturale suni göz yaşı eklenerek 25 mg/ml topikal damla elde edilir. Buzdolabında saklanır ve kullanmadan önce çalkalanarak kullanılır.
- Ceftazidim 50 mg/ml
- 1gr lık ilaç flakonunun içine 9.2 ml tears naturale eklenerek çözülür.
- Bu çözeltiden 5 ml alınıp, 5 ml tears naturale eklenerek elde edilir. Buzdolabında saklanır ve kullanmadan önce çalkalanarak kullanılır. Oda sıcaklığında 24 saat stabildir. Buzdolabında 96 saat stabil kalır.
- Amikacin 20 mg/ml
- 500mg/2ml lik ilaç 11.5 ml steril prezervan içermeyen su eklenerek 20 mg/ml solüsyon elde edilir. Buzdolabında saklanır ve kullanmadan önce çalkalanarak kullanılır.
- Gentamisin 15 mg/ml
- Paranteral 2ml/80 mg ampul direkt olarak 5 ml %0.3 lük gentamisin damla preparatının içine eklenerek hazırlanır.
- Tobramycin 15 mg/ml
- Paranteral 2ml/80 mg ampul direkt olarak tobramycin 5 ml %0.3 lük hazır damla preparatının içine eklenerek hazırlanır.
Fungal endoftalmilerde sistemik antifungal kullanımı
- Amphotericin B; 0.7-1 mg/kg/gün ( intravenöz olarak 2-6 saatte gidecek şekilde verilir.
- Fluconazole; 200mg/gün oral olarak tek seferde veya 2 ye bölerek kullanılır.
- Ketokonazol; 400mg/gün olarak tek seferde veya 2 ye bölerek kullanılır.
- Itraconazole; 200 mg/gün olarak tek seferde veya 2 ye bölerek kullanılır.
- Flucytosine: 50-100 mg/gün
- Varikonazol: 400mg/gün oral olarak tek seferde veya 2 ye bölerek kullanılır.
Cerrahi Tedavi
Endoftalminin cerrahi tedavisinde kanıta dayalı çalışma olarak tüm dünyada endoftalmi vitrektomi çalışması yol gösterici olmaktadır. Bu çalışmanın amacı endoftalmi gelişen olgularda 3 girişli vitrektomiyi intravitreal tap/biopsi ile karşılaştırmaktır.
Bu çalışmaya giriş kriterleri
- Sekonder göz içi lensi veya katarakt cerrahisinden sonra 6 hafta içerisinde endoftalmi gelişmiş olması.
- Önkamareda bulanıklık veya hipopiyon olması veya retina arteriollerinin net ve açık şekilde görülmesini engelleyen vitreus ortamının bulanık olması.
- Kornea ve ön kamaranın irisin bazı bölümlerinin görülmesini sağlayacak şekilde temiz olması.
- Korneanın pars plana vitrektomiye izin verecek şeffaflıkta olması.
- Görme keskinliğinin 20/50’ den kötü ancak en azından ışık persepsiyonunun olması
Bu çalışmanın sonuçları
- Sistemik antibiyotik kullanımının ortamın şeffaflığına veya sonuç görme keskinliğine hiçbir katkısı olmamıştır. Bununla beraber son çalışmalarda 4. Florokinolon grubu ilaçların (özellikle moxifloksasin) sistemik kullanımında endoftalmili olgularda ciddi miktarda vitreus boşluğuna geçtiği dolayısı ile etkili olduğu gösterilmiştir.
- El hareketleri veya daha iyi görme keskinliğine sahip olgularda acil pars plana vitrektomi ile tap/biopsi arasında fark bulunmamıştır. Bu sonuçlara rağmen 23g-25g-27g parsplana vitrektomi sistemleri ile daha iyi sonuçlar değişik yazarlar tarafından bildirimektedir.
- Işık persepsiyonu olan olgularda pars plana vitrektomi ameliyatlarının tap/bipsi grubuna oranla daha iyi görsel sonuçlar sağladığı tespit edilmiştir.
- 20/40 ve/veya daha fazla görme keskinliği, vitrektomi grubunda 3 kez daha fazla bulunmuştur (%33 vitrektomi, tap/biopsi %11)
- 20/100 ve/veya daha fazla görme keskinliği, vitrektomi grubunda 2 kez daha fazla bulunmuştur (%56 vitrektomi, tap/biopsi %30)
- 5/200 den daha az görme keskinliğine maruz kalma olasılığı, vitrektomi grubunda %20 tap/biopsi grubunda %47 olarak bulunmuştur.
Endoftalmi profilaksinde kendi uygulamamız
- Hasta cerrahiye hazırlanırken serviste; 5 dakika arayla 3 kez moxifloksasin damla uygulaması.
- Cerrahi öncesi hasta masaya alındığında topikal anestezik damla damlatılmasını takiben, moxifloksasin damla ve %10 luk betadin damlatılması.
- Cerrahi alanın %10 luk betadin ile dezenfekte edilmesi
- Yapışma özelliği iyi bir dreple kirpik ve kapak kenarları drep altında kalacak şekilde drepleme işlemi.
- %10’luk betadinle oküler yüzeyin yıkanması ardından bol BSS ile yıkanması ve betadinin uzaklaştırılması sonrası cerrahi işlem (cerrahi işlemlerde tüm malzemeler tek kullanımlık)
- Ameliyat sonunda önkameraya sefuroksim (Aprokam) uygulaması.
- Yara yeri kaçak kontrolü ve göz içi tonusunun ayarlanması (tonus biraz yüksek bırakılıyor ortalama 20-25 mm-hg)..
- Moxifloksasin göz damlası damlatılması ve ardından %5 lik 1-2 damla alt fornikse betadine damlatılması.
- Ameliyattan 2 saat sonra ilk gün 2 saat aralıklarla moxifloksasin göz damlası uygulaması.
- Ameliyat sonrası 1. gün moxifloksasin göz damlasının 4 hafta süre ile günde 4 kez damlatılması.
Not: Ameliyat sonrası medikal tedavide cerrahinin tipine göre antibiyotik damla dışında topikal olarak steroid damla ve non-steroid anti inflamatuar damlalarda kullanılmaktadır.
Cerrahi sonrası endoftalmi olgularına kendi yaklaşımımız (Fotoğraf 2)
- Göz içi cerrahi prensiplerine göre olgunun örnek alımı için hazırlanması.
- Ön kamara ve vitreustan yeteri kadar örneklerin alınması.
- Gram ve giemsa boyaması ve kültür antibiyogram yapılması (beyin kalp infüzyon besi yeri, thioglycollate besiyeri, kanlı agar besi yeri, çikolatalı agar, MacConkey agar ve Sabouraud agar besi yerlerine ekim)
- İntravitreal antibiyotik uygulaması (intravitreal uygulama dozlarında, vancomisin, seftazidim uygun görülürse dexametason) sistemik moxifloksasin uygulaması (400mg 1x1). Subkonjonktival vancomisin, seftazidim, gentamisin ve dexametazon uygulaması (subkonjonktival uygulama dozlarında). Topikal vancomisin ve moxifloksasin saat başı, sikloplejin 4x1, fortifiye gentamisin 8x1 (topikal uygulama dozlarında), uygun olgularda steroid damla 4x1. Kültür, antibiyogram ve klinik gidişat sonuçlarına göre ilaçlar yeniden düzenlenir.
- Bu uygulamaları takiben klinik gidişata göre 23 g parsplana vitrektomi silikonyağı uygulaması (fulminan gidişat, akut gidişat ve görme keskinliğinin el hareketlerine düşmüş olması durumlarında, görme keskinliğinin EVS kriterlerinde belirtilen ışık hissine düşmesi beklenmeden, kornea vitrektomi işlemine izin verecek durumda ise pars plana vitrektomi işlemi silikonyağı ugulaması, ameliyat sonunda vitreus boşluğuna uygun dozlarda vancomisin, seftazidim verilmesi, ön kamaraya sefuroksim ve moxifloksasin antibiyotik verilmesi, subkonjonktival vancomisin, gentamisin, dexametazon ve sefuroksim uygulaması, topikal uygun dozda; vancomisin ve moxifloksasin saat başı sikloplejin 4x1 fortifiye gentamisin 8x1, uygun olgularda steroid damla 4x1 şeklinde bir yaklaşımımız olmaktadır.
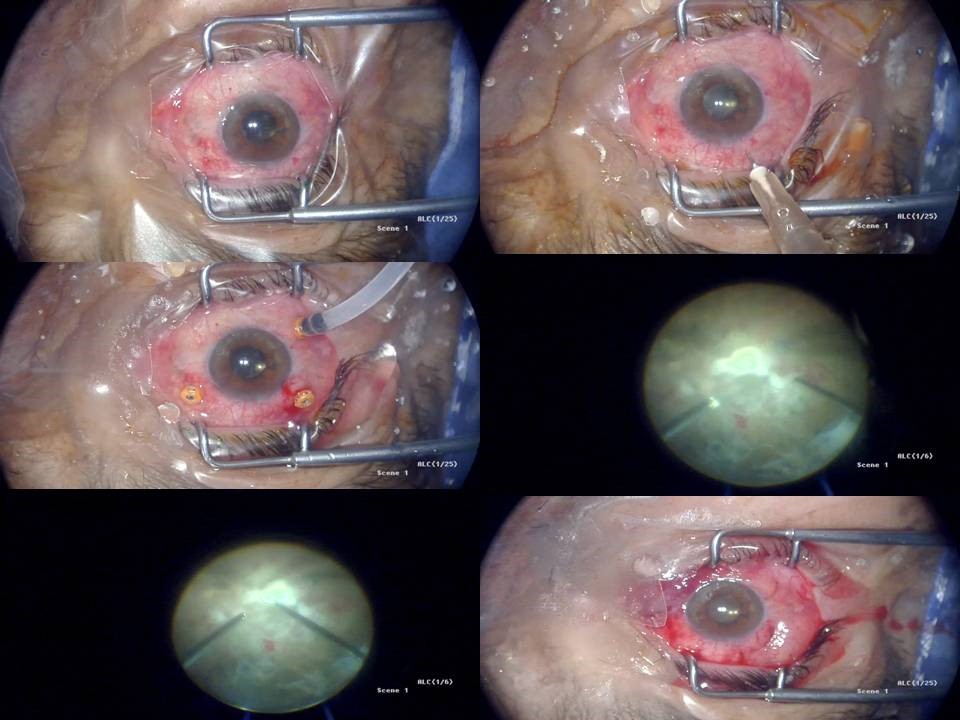
Fotoğraf 2: Diyabetik vitrektomi sonrası silikon yağı alımını izleyen 2. günde gelişen akut endoftalmi olgusu. (Ameliyat öncesi 27 g iğne ile vitreus sıvısı alımı, 3 girişimli vitrektomi işlemi, retinada bulanık görünüm, periflebit ve retina yüzeyinde beyaz kremsi membranlar, ameliyat bitimi görünümü)
Not: Bu endoftalmi olgusunda kendi yaklaşımımız sonucu (bak: sayfa 24); olguda gerek gram giemsa boyamalarda gerekse örneklerin besiyerleri değerlendirilmesinde üreme olmadı. (önkamera sıvısı, vitreus sıvısı ve vitrektomi kaset örneklerinde) Ameliyat sonrası takiplerde düzeltilmiş görme keskinliği 0.2, vitreus boşluğu temiz ve tedavi tam yanıt alındı.
KAYNAKLAR
- Speaker MG, Menikoff JA. Prophylaxis of endophthalmitis with topical povidone-iodine. Ophthalmology 1991:98:1769-1774.
- Boes DA, Lindquist TD, Fritsche TR, Kalina RE. Effects of povidone-iodine chemical preparation and saline irrigation on the perilimba flora. Ophthalmology 1992:99:1569-1574.
- Ciulla TA, Starr MB, Masket S. Bacterial endophthalmitis prophylaxis for cataract surgery: an evidence-based update. Ophthalmology 2002;109:13–24.
- Nentwich MM, Ta CN, Kreutzer TC, Li B, Schwarzbach F, Yactayo-Miranda YM, et al. Incidence of postoperative endophthalmitis from 1990 to 2009 using povidone-iodine but no intracameral antibiotics at a single academic institution. J Cataract Refract Surg 2015; 41:58–66.
- Barry P, Seal DV, Gettinby G, Lees F, Peterson M, Revie CW. ESCRS Endophthalmitis Study Group. ESCRS study of prophylaxis of postoperative endophthalmitis after cataract surgery: Preliminary report of principal results from a European multicenter study. J Cataract Refract Surg. 2006;32:407-10.
- Chang DF, Braga-Mele R, Henderson BA, Mamalis N, Vasavada A. ASCRS Cataract Clinical Committee. Antibiotic prophylaxis of postoperative endophthalmitis after cataract surgery: Results of the 2014 ASCRS member survey. J Cataract Refract Surg 2015; 41:1300–5.
- Ravindran RD, Venkatesh R, Chang DF, Sengupta S, Gyatsho J, Talwar B. Incidence of post-cataract endophthalmitis at Aravind Eye Hospital: outcomes of more than 42,000 consecutive cases using standardized sterilization and prophylaxis protocols. J Cataract Refract Surg 2009; 35:629–36.
- Ta CN, Egbert PR, Singh K, Shriver EM, Blumenkranz MS, Miño De Kaspar H. Prospective randomized comparison of 3-day versus 1-hour preoperative ofloxacin prophylaxis for cataract surgery. Ophthalmology 2002; 109:2036–40.
- Seal DV, Barry P, Gettinby G, Lees F, Peterson M, Revie CW, et al. ESCRS study of prophylaxis of postoperative endophthalmitis after cataract surgery: Case for a European multicenter study. J Cataract Refract Surg 2006; 32:396–406.
- Dong Y, Zhao X, Domagala J, Drlica K. Effect of fluoroquinolone concentration on selection of resistant mutants of Mycobacterium bovis BCG and Staphylococcus aureus. Antimicrob Agents Chemother 1999; 43:1756–8.
- Price FW, Dobbins K, Zeh W. Penetration of topically administered ofloxacin and trimethoprim into aqueous humor. J Ocul Pharmacol Ther Off J Assoc Ocul Pharmacol Ther 2002; 18:445–53.
- Bucci FA. An in vivo study comparing the ocular absorption of levofloxacin and ciprofloxacin prior to phacoemulsification. Am J Ophthalmol 2004; 137:308–12.
- Vasavada AR, Gajjar D, Raj SM, Vasavada V. Comparison of 2 moxifloxacin regimens for preoperative prophylaxis: prospective randomized triple-masked trial. Part 1: aqueous concentration of moxifloxacin. J Cataract Refract Surg. 2008; 34:1379–82.
- Barry P, Behrens-Baumann W, Pleyer U, Seal D. ESCRS Guidelines on prevention, investigation and management of post-operative endophthalmitis. Version. 2007;2:1–36.
- Behndig A, Cochener B, Güell JL, Kodjikian L, Mencucci R, Nuijts RMMA, et al. Endophthalmitis prophylaxis in cataract surgery: Overview of current practice patterns in 9 European countries. J Cataract Refract Surg 2013; 39:1421–31.
- Starr MB. Prophylactic antibiotics for ophthalmic surgery. Surv Ophthalmol. 1983; 27:353–73.
- Endophthalmitis Study Group, European Society of Cataract & Refractive Surgeons. Prophylaxis of postoperative endophthalmitis following cataract surgery: results of the ESCRS multicenter study and identification of risk factors. J Cataract Refract Surg 2007; 33:978–88.
- Shorstein NH, Winthrop KL, Herrinton LJ. Decreased postoperative endophthalmitis rate after institution of intracameral antibiotics in a Northern California eye department. J Cataract Refract Surg. 2013; 39:8–14.
- García-Sáenz MC, Arias-Puente A, Rodríguez-Caravaca G, Bañuelos JB. Effectiveness of intracameral cefuroxime in preventing endophthalmitis after cataract surgery Ten-year comparative study. J Cataract Refract Surg 2010; 36:203–7.
- Barreau G, Mounier M, Marin B, Adenis J-P, Robert P-Y. Intracameral cefuroxime injection at the end of cataract surgery to reduce the incidence of endophthalmitis: French study. J Cataract Refract Surg. 2012; 38:1370–5.
- Tan CSH, Wong HK, Yang FP. Epidemiology of postoperative endophthalmitis in an Asian population: 11-year incidence and effect of intracameral antibiotic agents. J Cataract Refract Surg. 2012; 38:425–30.
- Lam PTH, Young AL, Cheng LL, Tam PMK, Lee VYW. Randomized controlled trial on the safety of intracameral cephalosporins in cataract surgery. Clin Ophthalmol Auckl NZ. 2010; 4:1499–504.
- Lane SS, Osher RH, Masket S, Belani S. Evaluation of the safety of prophylactic intracameral moxifloxacin in cataract surgery. J Cataract Refract Surg. 2008; 34:1451–9.
- Espiritu CRG, Caparas VL, Bolinao JG. Safety of prophylactic intracameral moxifloxacin 0.5% ophthalmic solution in cataract surgery patients. J Cataract Refract Surg 2007; 33:63–8.
- Arbisser LB. Safety of intracameral moxifloxacin for prophylaxis of endophthalmitis after cataract surgery. J Cataract Refract Surg. 2008; 34:1114–20.
- Rudnisky CJ, Wan D, Weis E. Antibiotic choice for the prophylaxis of post-cataract extraction endophthalmitis. Ophthalmology. 2014; 121:835–41.
- Aaberg TM Jr, Flynn HW Jr, Schiffman J, Newton J. Nosocomial acute-onset postoperative endophthalmitis survey. Ophthalmology 1998: 105:1004–1010.
- Javitt JC, Vitale S, Canner JK, et al. National outcomes ofcataract extraction: endophthalmitis after inpatient surgery. Arch Ophthalmol 1991: 109:1085–1089.
- Powe NR, Schein OD, Gieser SC, et al. Synthesis of the literatüre on visual acuity and complications after cataract extraction with intraocular lens implantation. Arch Ophthalmol 1994: 112:239–252.
- Cohen SM, Flynn HW Jr., Murray TG, et al. Endophthalmitis after pars plana vitrectomy. Ophthalmology 1995: 102:705–712.,
- Egger SF, Huber Spitzy V, Scholda C, et al. Bacterial contamination during extracapsular cataract extraction. Prospective study on 200 consecutive patients. Ophthalmologica 1994:208:77–81.
- Gelender H, Flynn HW Jr, Mandelbaum SH. Bacterial endophthalmitis resulting from radial keratotomy. Am J Ophthalmol 1982: 93:323–326.
- Salamon, S.M., Friberg, T.R., Luxembourg, M.N. Endophthalmitis after strabismus surgery.Am J Ophthalmol. 1982;93:39.
- Greenfield DS, Suner IF, Miller MP, et al. Endophthalmitis after filtering surgery with mitomycin-C. Arch Ophthalmol 1996: 114:943–949.
- Kattan HM, Flynn HW Jr, Pfugfelder SC, et al. Nosocomial endophthalmitis survey: current incidence of infection after intraocular surgery. Ophthalmology 1991: 98:227–238.
- Çankaya C, Cumurcu T, Doganay S, Acinetobacter Baumannii endophthalmitis following intravitreal ranibizumab injection Ret-Vit 2013;21:59-62.
- Olson JC, Flynn HW Jr, Forster RK, et al. Results in the treatment of postoperative endophthalmitis. Ophthalmology 1983: 90:692–699.
- Pettit TH, Olson RJ, Foos RY, et al. Fungal endophthalmitis after intraocular lens implantation. Arch Ophthalmol 1980: 98: 1025–1039.
- Stern WH, Tamura E, Jacobs RA, et al. Epidemic postsurgical Candida parapsilosis endophthalmitis. Ophthalmology 1985: 92:1701–1709.
- Weissgold DJ, Maguire AM, Brucker AJ. Management of postoperative Acremonium endophthalmitis. Ophthalmology 1996: 103:749–756.
- Stern GA, Engel HM, Driebe WT. The treatment of postoperative enophthalmitis. Ophthalmology 1989: 96:62–67.
- Winward KE, Pflugfelder SC, Flynn HW Jr, et al. Postoperative propionibacterium endophthalmitis. Treatment strategies and long term results. Ophthalmology 1993: 100:447–451.
- Doft BH: Endophthalmitis vitrectomy study. Arch Ophthalmol 1991: 109:487–489.
- Han DP, Wisniewski SR, Wilson LA, et al. Spectrum and susceptibilities of microbiologic isolates in the Ednophthalmitis Vitrectomy Study. Am J Ophthalmol 1996:122:1–17
- Ormerod LD, Ho DD, Becker LE, et al. Endophthalmitis caused by the coagulase-negative staphylococci. Ophthalmology 1993:100:715–723.
- Johnson MW, Doft BH, Kelsey SF, et al. The Endophthalmitis Vitrectomy Study Group. Relationship between clinical presentation and microbiologic spectrum. Ophthalmology 1997: 104:261–272.
- Speaker MG, Milch FA, Shaf MK, et al. Role of external bacterial flora in the pathogenesis of acute postoperative endophthalmitis. Ophthalmology 1991: 98:639–64.
- Morris R, Camesasca FI, Byrne J, et al. Postoperative endophthalmitis resulting from prosthesis contamination in a monocular patient. Am J Ophthalmol 1993: 116:346–349.
- Phillips WB, Tasman WS. Postoperative endophthalmitis inassociation with diabetes mellitus. Ophthalmology 1994: 101: 508–518.
- Good WV, Hing S, Irvine AR, et al. Postoperative endophthalmitis in children after cataract surgery. J Pediatr Ophthalmol Strabismus 1990: 27:283–285.
- Wilson FM II. Causes and prevention of endophthalmitis. Int Ophthalmol Clin 1987: 27:67–73
- Sunaric Mégevand G, Pournaras CJ. Current approach to postoperative endophthalmitis. Br J Ophthalmol 1997: 81:1006–1015.
- Scott IU, Flynn HW Jr, Feuer W. Endophthalmitis after secondary intraocular lens implantation. A case-control study. Ophthalmology 1995: 102:1925–1931.
- Menikoff JA, Speaker MG, Marmor M, Raskin EM. A casecontrol study of risk factors for postoperative endophthalmitis. Ophthalmology 1991: 98:1761–1768.
- Hughes DS, Hill RJ.: Inectious endophthalmitis after cataract surgery. Br J Ophthalmol 1994: 78:227–232.
- Staudenmaier C. Current views on the prevention of postoperative infectious endophthalmitis. Can J Ophthalmol 1997: 32:297–302.
- Donnenfeld ED, Perry HD. Cataract surgery: 5 ways to prevent endophthalmitis. Rev Ophthalmol 1996: Jan:67–72.
- Amon M, Menapace R. Long-terms results and biocompatibility of heparin-surface-modified intraocular lenses. J Cataract Refract Surg 1993: 19:258–262.
- Liesegang TJ. Prophylactic antibiotics in cataract operations. Mayo Clin Proc 1997: 72:149–159.
- Katz LJ, Cantor LB, Spaeth GL. Complications of surgery in glaucoma. Early and late bacterial endophthalmitis after glaucoma filtering surgery. Ophthalmology 1985: 92:959–963.
- Mandelbaum S, Forster RK, Gelender H, et al. Late onset endopthalmitis associated with filtering blebs. Ophthalmology 1985: 92:964–972.
- Tabbara KF. Late infections after filtering procedures. Ann Ophthalmol 1976: 8:1228–1231.
- Wolner B, Liebmann JM, Sassani JW, et al. Late blebrelated endophthalmitis after trabeculectomy with adjunctive 5-fluorouracil. Ophthalmology 1991: 98:1053–1060
- Ayyala RS, Stevens SX, Grizzard WS, Fouraker BD. Recurrent endophthalmitis after cataract surgery with a scleraltunnel incision. Cornea 1998: 17:233–235.
- Ormerod LD, Puklin JE, McHenry JG, McDermott ML. Scleral flap necrosis and infectious endophthalmitis after cataract surgery with a scleral tunnel incision. Ophthalmology 1993: 100:159–163.
- Kanellopulos AJ, Dreyer EB. Postoperative infection after current cataract extraction surgery. Postoperative infection after current cataract extraction surgery. Int Ophthalmol Clin 1996: 36:97–107.
- Fox G, Joondeph BC, Flynn HW Jr, et al. Delayed-onset pseudophakic endophthalmitis. Am J Ophthalmol 1991: 111:163–173
- Smith RE. Inflammation after cataract surgery. Am J Ophthalmol 1986: 102:788–790
- Meisler DM, Mandelbaum S. Propionibacterium-associated endophthalmitis after extracapsular cataract extraction. Ophthalmology 1989: 96:54–61.
- Chien AM, Raber IM, Fischer DH. Propionibacterium acnes endophthalmitis after intracapsular cataract extraction. Ophthalmology 1992: 99:487–490.
- Borne MJ, Elliot JH, O’Day DM. Ocular fluconazole treatment of Candida parapsilosis endophthalmitis after failed intravitreal amphotericin B. Arch Ophthalmol 1993: 111:1326–1327.
- Jaffe NS. Cataract Surgery and Its Complications. St Louis, CV Mosby, 1984, ed 4, p 507
- Kattan HM, Flynn HW Jr, Pfugfelder SC, et al. Nosocomial endophthalmitis survey: current incidence of infection after intraocular surgery. Ophthalmology 1991: 98:227–238.
- Ciulla TA, Beck AD, Topping TM, Baker AS. Blebitis, early endophthalmitis and late endophthalmitis after glaucoma filtering surgery. Ophthalmology 104:986–995, 1997.
- Hattenhauer JM, Lipisich MP. Late endophthalmitis after filtering surgery. Am J Ophthalmol 1971: 72:1097–1101.
- Kangas TA, Greenfield DS, Flynn HW Jr, et al. Delayed onset endophthalmitis associated with conjunctival filtering blebs. Ophthalmology 1997: 104:746–752.
- Higginbotham EJ, Stevens RK, Musch DC, et al. Bleb related endophthalmitis after trabeculectomy with mitomycin C. Ophthalmology 1996: 103:650–656.
- Mandelbaum S, Forster RK. Endophthalmitis associated with filtering blebs. Int Ophthalmol Clin 1987: 27:107–111.
- Mandelbaum S, Forster RK, Gelender H, et al. Late onset endopthalmitis associated with filtering blebs. Ophthalmology 1985: 92:964–972.
- Higginbotham EJ, Stevens RK, Musch DC, et al. Bleb related endophthalmitis after trabeculectomy with mitomycin C. Ophthalmology 1996: 103:650–656.
- Krebs DB, Liebmann JM, Ritch R, et al. Late infectious endophthalmitis from exposed glaucoma setons. Arch Ophthalmol 1992: 110:174–175.
- Perkins TW. Endophthalmitis after placement of a Molteno implant. Ophthalmic Surg 1990: 21:733–734.
- Donahue SP, Kowalski RP, Jewart BH, Friberg TR. Vitreous cultures in suspected endophthalmitis. Biopsy or vitrectomy? Ophthalmology. 1993;100:452-455.
- Sharma S, Jalali S, Adiraju MV, et al. Sensitivity and predictability of vitreous cytology, biopsy, and membrane filter culture in endophthalmitis. Retina. 1996;16:525-529.
- Microbiologic factors and visual outcome in the endophthalmitis vitrectomy study. Am J Ophthalmol. 1996;122:830-846.
- Cornut PL, Boisset S, Romanet JP, et al. Principles and applications of molecular biology techniques for the microbiological diagnosis of acute post-operative endophthalmitis. Surv Ophthalmol. 2014;59:286-303.
- Chiquet C, Maurin M, Thuret G, et al. Analysis of diluted vitreous samples from vitrectomy is useful in eyes with severe acute postoperative endophthalmitis. Ophthalmology. 2009;116:2437-2441.

